子どものがんで一番多いのは急性リンパ性白血病という名前の白血病です。研究が進むとともにどんどん治療成績が改善しており、現在では90%の確率で治ります。私たちは、残りの10%、すなわち治らなかった急性リンパ性白血病を調べた結果、そこに90%の確率で治らない白血病が潜んでいたことを発見しました。
急性リンパ性白血病(Acute Lymphoblastic Leukemia、ALL)は、小児期において最も頻度が高い血液がんで、日本では1年間に約500人の小児が新たに発症します。すべての小児がんを合わせて年間2,000人なので、ALLが占める割合はとても大きいです。
このタイプの白血病は、治療成績がどんどん改善した病気の1つです。ここ40年程の間に、以前は50%ほどだった治癒の可能性が、現在は約90%まで改善しました。これに役立ったのは、悪性度(白血病の強さ)に基づいた適切な強さの治療(層別化治療)、複数の抗がん剤を組み合わせた治療(多剤併用化学療法)の改良、骨髄移植などの造血幹細胞移植の導入です。しかしながら、一旦病気が再発した患者では、依然として状況は厳しいです。
ALLは様々な遺伝子の変異を伴って発症することが知られており、それによって治療法が変わります。例えば、BCR-ABL1融合遺伝子という異常な遺伝子を持つALLは、かつては治療することが非常に困難でした。しかし、チロシンキナーゼ阻害薬という、BCR-ABL1に特別によく効く薬(分子標的薬)を使うようになって、劇的によく治るようになりました。
依然として、ALLを起こす遺伝子の異常は全てが解明されているわけではありません。近年飛躍的に進歩した、遺伝子解析の方法を使って、ALLにおける新しい遺伝子の異常を見つけることを計画しました。新しい遺伝子の異常が見つかれば、より適切な悪性度の決定(リスク層別化)、新しい治療薬の使用・開発が可能になり、さらに治療成績がよくなると期待されます。
私たちは、再発したALL、あるいは最初の治療が効かなかったALLを59人分、次世代シーケンサーという遺伝子解析装置を用いて調べました。その結果、4人において、MEF2D遺伝子とBCL9遺伝子という2つの別々に存在すべき遺伝子がくっついてしまっていることを見つけました(MEF2D-BCL9融合遺伝子)。この2つの遺伝子は、人間の設計図の中で、かなり近い場所に位置しており、ちょっとした間違いによってつながってしまいやすい状況にありました。また、近い場所で起こるちょっとした間違いなので、これまで病院で行われてきた遺伝子の検査法では検出できないことがわかりました。
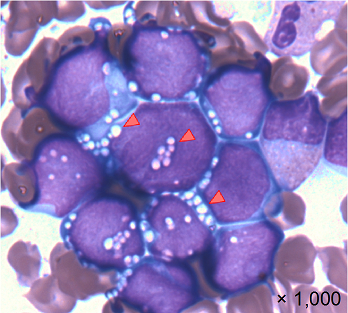
MEF2D-BCL9融合遺伝子をもつ白血病は、10歳以降の発症(多くのALLは2歳頃に発症します)、B前駆細胞性という分類、白血病細胞の中に空気の泡のようなものが見える(空胞を持つ)、従来の抗がん剤治療が効きにくく、抗がん剤治療中にも関わらず再発する、などの特徴がありました。結果として、MEF2D-BCL9融合遺伝子が見つかった白血病の子どもは、全員が亡くなっていました。すなわち、MEF2D-BCL9融合遺伝子は、悪性度の高いALLを起こすと考えられます。
なぜこの融合遺伝子があると悪性度の高いALLが起こるのか、あるいは治療するにはどうしたらいいかを調べるため、患者さんの白血病細胞を、試験管の中で培養できるようにしたもの(細胞株)を作り、実験しました。その結果、MEF2D-BCL9融合遺伝子があると、白血病細胞の増殖が速くなることに加えて、ALL治療の鍵となる副腎皮質ステロイド薬がほとんど効かなくなることがわかりました。 その一方で、薬剤感受性試験の結果からは、ヒストン脱アセチル化酵素阻害剤やプロテアソーム阻害剤など、すでに他のがん、あるいは他の白血病では実用化されている分子標的薬の効果が期待できることが示されました。
この研究により発見され、その機能が明らかとなったMEF2D-BCL9融合遺伝子は、悪性度の高い白血病であることを示す指標であり、治療方針の決定に役立つと考えられます。また、この融合遺伝子を持つ白血病に対して新しい治療法を開発することで、ALLの治療成績が向上すると期待されます。この研究は、がん研究において最も権威ある雑誌の1つであり、米国臨床腫瘍学会(ASCO)の学会誌である、Journal of Clinical Oncology誌に掲載されました。